- ホーム
- 診療科・部門のご案内
- 救急科 診療科・部門のご案内
- 中毒通信
救急科
中毒通信
消化管除染の適応について
消化管除染といえば中毒診療の「基本のき」ですが、実際にどうやって消化管除染の方法を選択するか考えたことがありますか?
つい最近、消化管除染についてのReviewが出ていたので、参考になればとまとめました。
胃洗浄
命に関わる中毒で、摂取後の時間経過が短く、胃内に毒物が残っている場合に適応になります。
有効な拮抗薬がある(オピオイド、アセトアミノフェンなど)、活性炭によく吸着される物質には胃洗浄は避ける傾向にあります。
32−36frと太いチューブを使って1回量250−500mlの温水で洗浄(小児では22−28Frで15ml/kgの温かい生食)で胃内容物がきれいになるまで洗浄します。左側臥位にして幽門から先に薬物が流れないように注意します。
このように太いチューブを使うので、挿管されていない患者ではまず胃洗浄は難しいです。
活性炭
活性炭投与には、活性炭単回投与(SDAC:Single Dose Activated Charcoal)と活性炭追加投与(ADAC:Additional Dose Activated Charcoal)、活性炭複数回投与(MDAC:Multiple Dose Activated Charcoal)があります。MDACは腸透析とも言われ、腸肝循環する薬剤を腸管内で吸着し、便中に排泄させることで排泄を促進する特徴があるので若干性質がことなります。
通常はSDAC(単回投与)が行われますが、大量摂取による中毒(吸着には薬毒物の10倍料の活性炭が必要)や、徐放錠で吸収が続いているような場合では活性炭の投与量を増やすためにADAC(追加投与)をすることもあります。
活性炭は自分で飲める場合には飲んでもらいます。
腸洗浄
大腸カメラの前処置で使うボリエチレングリコールを服用して、腸管を洗い流す方法です。活性炭が無効な物質(鉄やリチウムなど)、幽門を通過してしまった中毒、リスクの高い徐放錠の中毒、胃洗浄のチューブを通らないものなどで使用されます。
その他
内視鏡や開腹手術などもありますが、ごく例外的な方法です。
時間の考え方
以前は「消化管除染は1時間以内」とされていましたが、最近では1時間を超えても胃内に薬物が残っている可能性があること、また活性炭では1時間以上経過していても有効性を示唆するデータがあることから、1時間の壁については厳密に捉えず比較的リベラルに消化管除染を行ってもいいように思えます。ただ、活性炭についてはデータも多少はありますが、胃洗浄については裏付けとなるデータはあまりありません。オーストラリアのガイドラインでは通常なら2時間以内、徐放錠なら4時間以内としています。
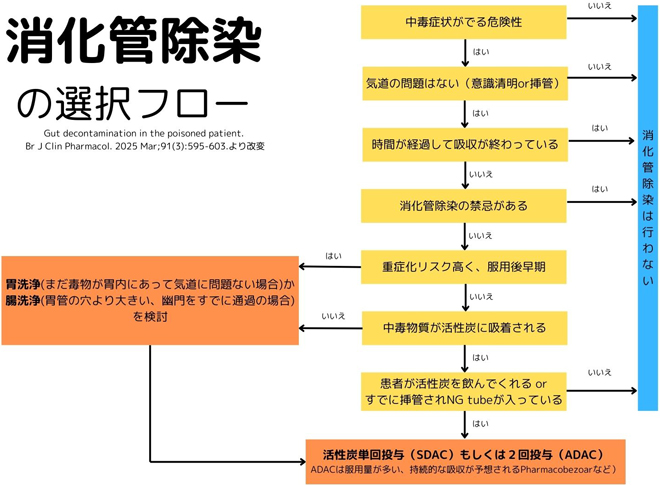
参考までに消化管除染の選択について図を示します。
パラコート中毒
パラコート中毒は除草剤の中でも極めて致死的なものです。過去にはパラコートが20%含まれる製剤が取り扱われていましたが、あまりに危険であるとして現在は5%の製剤しか発売されていません。またパラコートと同じ系統の薬剤(ビピリジニウム系)としてジクワットがあり、ジクワットとパラコートが混ざった製剤が販売されています。
パラコートは健常な皮膚からの吸収はあまりなく、吸入により暴露もあまり問題になりません。消化管からの吸収はたったの5%程度ではあるのですが、それでも20%製剤を5−10ml服用しただけで致死的になりえます。パラコート中毒の死亡率は50−90%ですが、自殺企図で多量に服用した場合には死亡率はほぼ100%と言われています。吸収された後は代謝されることなく腎臓で排泄されます。腎機能が維持されていれば1時間ぐらいで血中濃度がピークになりその後低下します。パラコートは肺胞上皮細胞に親和性があり、肺に分布します。そのため肺胞の障害および線維化が起こりやすくなります。(ジクワットはあまり肺の障害を起こしません。)パラコートもジクワットも腎機能障害は起こし、腎機能障害を起こすと排泄の遅延が起きてしまうため、その毒性が高まります。障害のメカニズムとしてはフリーラジカルを産生しての非特異的な細胞の障害・壊死になります。
服用後早期から消化管の腐食による症状が出現します。消化管穿孔を起こすと極めて予後が不良です。また腎不全は5日程度をピークにして生存例では数週間で改善します。肝機能障害が出現することもあります。呼吸不全・ARDS・肺の線維化は徐々に進行して数週間から数ヶ月で悪化してきます。生存例では数年かけて改善するとも言われています。20%のパラコートを50−100ml服用すると数日の経過で多臓器不全に至り亡くなると報告されています。ノモグラムがありそれにより死亡率を推定することが可能とされていますが、実臨床では血中濃度をそれほど早期に測定できるわけではないので、ノモグラムの使用については制限があります。
残念ながら特異的な治療があるわけではありません。確率したエビデンスがあるわけではありませんが、早期(4−6時間以内)の血液浄化療法ができるなら、予後改善効果があるかもしれないという報告もあります。血液浄化療法を行うなら、血液灌流(Hemoperfusion)の方が効果的と言われていますので、活性炭カラムがある場合はそれを使用することを検討してもよいと思います。
ボツリヌス中毒
最近、新潟でで食品由来と思われる成人のボツリヌス中毒がニュースになりました。ボツリヌス中毒は発症頻度が低いため遭遇することは少ないですが、重篤化すると呼吸麻痺を引き起こし、致命的となることがあり要注意な中毒です。
ボツリヌス中毒は、ボツリヌス神経毒素(BoNT)による神経筋伝達障害を引き起こす疾患です。原因は Clostridium botulinumなどの細菌が産生する毒素です。最も強力な神経毒の一つで、致死量は0.001μg/㎏とも言われています。BoNTはアセチルコリンの放出を阻害し、進行性の筋弛緩性麻痺を引き起こします。
ボツリヌス中毒は、食品由来、乳児ボツリヌス症、創傷ボツリヌス症、成人腸管定着型・医原性ボツリヌス症などのタイプに分類されます。食品由来ボツリヌス中毒は、瓶詰め食品や発酵食品などに含まれるボツリヌス毒素を摂取することで発症します。日本ではいずしによる発症が多く報告されています。乳児ボツリヌス症は、ボツリヌス菌の芽胞を摂取し、腸内で増殖して毒素を産生することで発症します。はちみつの摂取などが原因になるとされていますが、原因不明のこともあります。創傷ボツリヌス症は、傷口にボツリヌス菌が感染し、局所で毒素が産生されることによって起こります。その他にボツリヌス症は、ボツリヌス毒素をエアロゾルとして吸入することで発症し、生物兵器としてのリスクも指摘されていたり、美容などにも使われるボトックス投与によって発症したりすることがあります。
ボツリヌス中毒の診断では、神経症状の特徴を把握することが重要です。患者の意識や感覚は正常であるものの、対称性の進行性筋弛緩性麻痺が認められます。初期には複視や眼瞼下垂、嚥下障害や構音障害などの球麻痺症状が出現し、次第に四肢麻痺へと進行します。重症化すると呼吸筋麻痺を引き起こすため、迅速な対応が求められます。ギランバレー症候群が抹消から中枢に移行していくのと反対になりますが、フィッシャー症候群などとは臨床的には鑑別が難しいかもしれません。診断は通常の病院では難しく、保健所経由で依頼することになります。Mouse Lethality Assayといってマウスにサンプルと抗毒素を同時に投与した場合とサンプルのみを投与した場合で症状をみて判断するというのが最終的な診断になり、診断までには多少の時間がかかります。
治療の基本は支持療法と抗毒素療法です。最も重要なのは呼吸管理であり、重症例では気管挿管や人工呼吸管理が必要となる場合があります。抗毒素療法は食品由来、創傷、吸入性ボツリヌス症に適応されます。馬由来の血清でありアナフィラキシーのリスクがあります。適切な呼吸管理と治療が行われれば死亡率は低下しますが、回復にはかなり時間がかかります。
浸透圧ギャップにおけるエタノールの項の除数は何が適切か?
浸透圧ギャップの計算には、エタノールの影響を考慮するために3.7または4.6で割る方法が提案されています。浸透圧の計算式は以下の通りです。
2×Na(mEq/L) + Glucose(mg/dL)/18 + BUN(mg/dL)/2.8 + Ethanol(mg/dL)/3.7
または
2×Na(mEq/L) + Glucose(mg/dL)/18 + BUN(mg/dL)/2.8 + Ethanol(mg/dL)/4.6
ここで、エタノールの項の除数 が3.7または4.6のどちらが適切かが問題になります。
2001年の研究(1)ではER患者を対象に3.7が最適とされましたが、つい最近の研究(2)では、健康なボランティアにエタノールを摂取させ、浸透圧を測定した結果、4.6の方が正確性が高いことがわかりました。
浸透圧ギャップは以下の式で計算されます。
浸透圧ギャップ = 実測浸透圧 ― 計算浸透圧
3.7を使用すると計算浸透圧が高めに出るため、浸透圧ギャップが低く見積もられ、有毒アルコール中毒の見逃しにつながる可能性があります。偽陽性が増えるけれど、偽陰性が減るわけです。
スタディーを見比べてみると、実際の救急患者には3.7が適しているかもしれませんが、より慎重な対応をするために4.6の使用が望ましいように思えます。
浸透圧ギャップの使用そのものについても議論の余地がありますが、今回の結果をみて浸透圧ギャップを使用する場合は4.6を除数として使用するのがいいのではと考えています。
参考文献
- Purssell RA, Pudek M, Brubacher J, Abu-Laban RB. Derivation and validation of a formula to calculate the contribution of ethanol to the osmolal gap. Ann Emerg Med. 2001;38(6):653-659. doi:10.1067/mem.2001.119455
- Marino R, Sidlak A, Scoccimarro A, Flickinger K, Pizon A. Ethanol and the Limitations of the Osmol Gap. Annals of Emergency Medicine. 2025;0(0). doi:10.1016/j.annemergmed.2024.12.022
2024年の中毒カンファレンス
2024年も1年間を通じて毎月中毒カンファレンスを行いました。
様々な症例を通じていろんな中毒を学んだ1年でした。
hot cold reversalといえば?
CO中毒の高気圧酸素療法の適応は?
発毛クリニックに行った患者が低血圧?原因は?
除草剤を飲んだみたいだけど、何故か乳酸値が高い?一体なぜ?
1年を通じて参加して、こんな質問もすらすら答えられるようになった?
2025年も中毒カンファを通じて皆さんが勉強できるように頑張ります。
参考までに2024年の勉強会で取り扱ったテーマをあげておきます。見ているだけでどんな症状でどう治療すればいいか、想像力を掻き立てられます。
- ナツメグ
- マグネシウム
- カンナビノイド
- デキストロメトルファン
- 一酸化炭素
- シガテラ
- カルシウムチャネル機構薬
- ミノキシジル
- リスペリドン
- エチレングリコール
- ラモトリギン
- 2,4-D

中間症候群(有機リン中毒)
皆様は有機リン中毒の合併症である中間症候群をご存知ですか?
中間症候群は、急性有機リン中毒後24〜96時間で現れ、遅発性筋力低下を特徴とします。特に頸部屈筋と呼吸筋に影響を与え、近位筋の筋力低下が目立ちます。多くの場合初期のコリン作動性の症状が解消した後に現れます。中枢神経の異常は伴わず、患者は低酸素脳症などの合併症が生じない限り意識は保たれています。
神経筋接合部機能不全が病態の本態とされています。有機リン中毒によるコリンエステラーゼ阻害が神経筋接合部にアセチルコリンが過剰な状態を作ります。それによる持続する神経筋接合部の刺激がダウンレギュレーションを引き起こすのが中間症候群の原因ではないかとされています。そのため農薬が体内から排除された後も回復に時間がかかり、長期間呼吸のサポートが必要になります。有機リンの種類によって中間症候群の起こりやすさは異なり、パラチオンなどで起こりやすくなります。
診断は主に臨床診断で、近位筋の筋力低下が鍵になります。電気生理学的検査で、シナプス前およびシナプス後の関与を示唆する徴候が見られることも参考になります。中間症候群の重症度とタイミングは、有機リンによるアセチルコリンエステラーゼの抑制の速度と程度によって影響を受けるとされています。
中間症候群は病初期にアセチルコリンエステラーゼの活性化が低い状態が続くことが原因とされています。パムは有機リンによる阻害されたらアセチルコリンエステラーゼを再活性化する作用があり、一部の研究ではパムによる十分な治療が行われないことが中間症候群に寄与していると示唆されていますが、マラチオンのようにパムにあまり反応しない有機リンではパムの効果は限定的です。また、残念ながら有機リン全体としてパムの有効性を示すエビデンスは強くありません。ただし、もし使うのであれば早期に十分な量を使うことが必要だと考えます。
HHCHヘキサヒドロカンナビヘキソール
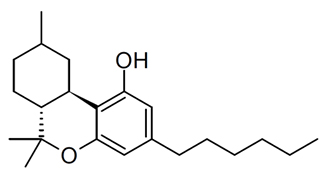
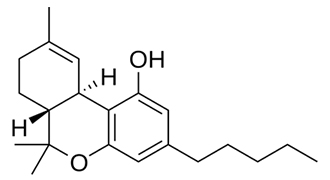
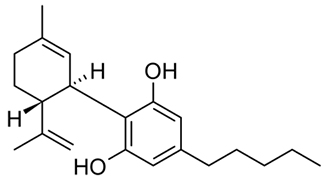
HHCHを含むグミを食べて体調不良になった方が多発した件についてニュースになっています。アルファベットが並んでぱっと見ただけでは何のことやらわかりにくいかもしれません。このHHCHの構造式を下記に示します。その隣に大麻の有効成分とされるTHC(テトラヒドロカンナビノール)を並べてみます。どれほど構造がよく似ているかわかるかと思います。THCは大麻に含まれる成分の中で最も精神症状をきたしやすい成分で、気分を高揚させる目的で大麻を使用する人はもっぱらこのTHCの効果を求めているとされており、最近の大麻は品種改良でこのTHC成分割合がどんどん増えています。また、これとは似た成分にCBD(カンナビジオール)があります。CBDも大麻に含まれる成分ですが、こちらはあまり精神作用をもたらさず、多幸感もあまり起こさないとされていて、一般的な治療として定着していないものの痙攣や難治性の疼痛に対する治療として効果があるのではと注目する方もいます。CBDを含むリキッドなども最近オンラインで購入できるようなものがあり、その後体調不良を訴えて病院を受診される方がいます。CBDについては比較的その作用や副作用が検証されていますが、HHCHについては正直その効果などあまり医学的に深く検証されているとは言えません。ということでHHCHそのものについての医学的問題点はまだあまり良くわからない状況ではあるのですが、今回のHHCHグミの事件を受けて考えられる問題点が3つほどあります。
①THC混入の可能性
もともとHHCHはTHCを原料にして合成されたものです。CBDもTHCもどちらも大麻に含まれるものです。というわけでよっぽど注意深く行わなければCBD純度100%、HHCH純度100%というのは難しいわけです。実際購入したCBD関連の製品にTHCが含まれていたという報告は多数上がっています。今回のHHCHもおそらくそうなのではと想像します。
②その他の薬毒物が紛れている可能性
ちゃんと監査が入っている製薬会社の薬であっても不純物が紛れて問題になることがあります。違法薬物の世界でははっきりとした理由はわかりませんが、不純物が紛れることがしばしばあります。最近は合成大麻に殺鼠剤が混じっていて、殺鼠剤の副作用で大出血を起こした症例が多発したことも報告されていますし、フェンタニルにXylazineという獣医が使う鎮静剤が紛れていたということも報告されています。安全な薬を作るには先人たちの大きな努力が払われているわけですが、こういったあまりしっかりと管理されていない製品には不純物が紛れていても分からず、それによって中毒症状がでる可能性もあります。
③経口摂取により中毒症状が遷延する可能性
大麻などカンナビノイドを摂取するには様々な方法がありますが、大きく分けてタバコのように吸入するという方法と、グミやチョコレートに混ぜて口から摂取するという方法があります。吸入する場合は薬物の体内での血中濃度が急激に上昇するので、摂取しすぎたら多くの人はすぐに摂取をやめるため、結果的に中毒量を大きく超えて薬物を摂取することは少ないです。(もちろん極めて毒性が高い合成カンナビノイドであれば別の話ですが。)ところが経口摂取した場合には血中濃度が上昇するまで時間がかかるため、結果的に血中濃度が中毒域に入ってきたころには胃の中に大量の薬毒物が入っていてその後も吸収され続けて症状が遷延するということがあります。大麻やその類似物質で入院となるのはほとんど経口摂取の場合です。患者様が病院を受診された場合にはどのような形でカンナビノイドを摂取したかというのも非常に重要な情報になり、経口摂取の場合には慎重な経過観察が必要になります。
アセトアミノフェン中毒の新しいガイドライン(米国・カナダ)
アセトアミノフェン中毒は欧米で肝障害の原因となる最もコモンな原因の一つです。
そのメカニズムおよび治療については下記のアセトアミノフェン中毒はなぜ起こる?をご参照ください。
基本的にアセトアミノフェンの血中濃度を服用後4−24時間の時点で測定して、ノモグラムの上にプロットして、その点が治療ラインよりも上であればNアセチルシステインで治療するということになります。Nアセチルシステインは米国・カナダでは点滴での治療になりますが(点滴であれば1日の入院ですむが、内服だと3日間なので)日本には注射製剤がないので内服のみになります。点滴での治療のレジメンのどれがいいのかも大きな議論の対象になって、今回もハイリスク患者では増量しましょうという推奨がでていますが、日本だと内服しかないので問題になりません。あとは治療終了をいつ行うべきかが明確になったというのが新しい点です。その他に抗コリン薬やオピオイドと併用した場合や肥満・妊婦などもコメントがつきました。ただ最近脚光を浴びているホメピゾールは特に今回のガイドライン ではコメントされているものの、立ち位置は明確になりませんでした。
今回はガイドライン で注目すべきポイントは以下の通りです。
<アセトアミノフェン急性中毒>
急性中毒の定義が曖昧であったのが、明確化されました。
最初にアセトアミノフェンの口にしてから24時間以内のプレゼンテーションすべて。何時間かけて服用していても良い。
ノモグラムに血中濃度をプロットするときの時間は最初の服用時間から数える。
<ノモグラムの変更>
肝障害ラインと治療ラインだったものが(それぞれ4時間後で200mcg/mlと150mcg/ml)
ハイリスクラインと治療ラインに(それぞれ4時間後で300mcg/mlと150mcg/ml)に変更になる。
<活性炭>
4時間以内なら投与 ハイリスク群(後述)なら4時間を超えていても検討
<ハイリスク群の定義>
30g以上の内服 または ノモグラムでハイリスクラインを超える
→活性炭を4時間超えていても投与検討、Nアセチルシステインを増量(経口投与の場合はすでに頚静脈投与よりかなり多いので増量しなくても良さそうではある)
→乳酸値、血ガスも評価。ミトコンドリア機能不全を起こしている可能性あり
<Nアセチルシステインの終了のクライテリア>
アセトアミノフェン血中濃度<10mcg/ml
臨床的に安定(肝性脳症があったり、腎不全が悪化していたりしない)
PT-INR<2
AST/ALTがピークから下がってきている(25−50%)
<慢性中毒の場合(24時間以上)>
アセトアミノフェン血中濃度<20mcg/ml かつ AST/ALT正常 なら治療不要
アセトアミノフェン血中濃度>20mcg/ml もしくは AST/ALTが異常なら治療
<長時間作用型のアセトアミノフェン・オピオイドや抗コリン薬との同時服用>
血中濃度がノモグラインの治療ライン以下でも4-6時間後に再検する
<体重100kg以上のとき>
Nアセチルシステインの計算は体重100kgとして計算しそれ以上増量しない。
<妊婦>
点滴Nアセチルシステインを好む中毒専門医もいるが、はっきりとしたデータない
<透析>
アセトアミノフェン血中濃度900mcg/mlを超えていて、アシドーシスや意識障害があるとき
*ホメピゾールはエビデンスが十分でなく役割はまだ明らかではない
2023年3月の中毒カンファレンス
2023年3月17日に中毒カンファレンスを行いました。
今回はテーマはミフクラギの中毒でした。聞いたことがない方も多いかもしれません。沖縄や亜熱帯地域に見られる植物で、観賞用としても売られています。
実がマンゴーのような外見をしていることからSea Mangoと言われることもありますが、実際はそのきれいな外観とは似つかわしくない猛毒を含み著明な心毒性をもたらします。
キョウチクトウの仲間でありジギタリスのような毒で、その毒成分はケルベリンという名前がついています。実際に南アジアでは自殺の木という物騒な名前もついています。
症例報告をめくると死亡例が次から次にでてくるかなり恐ろしい中毒になります。治療はジギタリスと同様です。
活性炭や胃洗浄が適応になれば行いますし、場合によっては循環不全に対してペーシングやVA−ECMOなどを考慮することになります。
ジギタリス中毒と同様に高カリウム血症にもなるのでそれに対しても対応が必要です。強心配糖体を含む植物としてその他にすずらん、キョウチクトウ、キツネノテブクロ、海葱(カイソウ)などがあります。
動物毒でもヒキガエルの毒ブフォトキシンも同じ強心配糖体を含みます。植物毒や動物毒もなかなか奥深い世界です。
エチレングリコール中毒の新ガイドラインとホメピゾール
2023年1月にエチレングリコール中毒について新しいガイドライン がでました。
エチレングリコールは1月の中毒カンファレンスでも取り上げましたが、不凍液に使われており、甘い味がするため小児の中毒も時折見られます。
ホメピゾールはエチレングリコールがアルコール脱水素酵素に代謝されて有毒な代謝産物(グリコアルデヒド、グリコール酸、シュウ酸など)に分解されるのを防ぎます。
エチレングリコールの状態で体内に残るだけであれば酩酊になるだけで大きな問題は起こさず、エチレングリコールそのものは腎臓から抜けていくので代謝をブロックしておけば大丈夫というわけです。
エチレングリコールが代謝されると有毒な代謝産物ができて代謝性アシドーシスになるわけですが、その前にホメピゾールを使うことができれば透析を避けることができるかもしれません。
逆にAGが27以上の代謝性アシドーシスがあるということはすでに有毒な代謝産物ができているということなので透析を行う必要があります。
細かい透析の適応についてはリンクのガイドラインを読んでみてください。AGの具体的な値が出てきたのが今回のガイドラインで新しく、そして臨床の現場でも役に立つところですね。
2023年2月の中毒カンファレンス
2023年2月17日に行われた中毒カンファレンスはトルエン中毒についてでした。
トルエンはシンナーの成分として使われ、昔はシンナー遊びとして吸入として乱用する方が多かったものです。
最近ではかなり少なくなっていますが、まだ現場で遭遇する疾患のようですね。
アニオンギャップの開大しない代謝性アシドーシスと低カリウム血症が診断の鍵になります。
シンナーなどは本人から自発的に使用歴を教えてくれないことが多いので、診察所見や採血結果などから診断につなげる意義は大きいです。
心筋のカテコラミンへの感受性が高まっていて、シンナー遊びをしている瞬間に警察官に見つかり追いかけられたりすると致死的な心室性不整脈がおこることがありSudden sniffing deathといわれています。
心室性不整脈は通常通り除細動や心臓マッサージなどで治療する必要があるのですが、面白いことにβ遮断薬を使用した方が効果的ではないかと言われています。
違和感を感じるかもしれませんが、Vfストームに対してβ遮断薬を使うことがあるのと似た話です。
2023年1月の中毒カンファレンス
2023年1月13日に中毒カンファレンスを行いました。テーマはエチレングリコール中毒でした。著明なアニオンギャップ開大の代謝性アシドーシスと浸透圧ギャップがあり、診断に至りました。一般にエチレングリコールは不凍液として使用されますが、古いアイスノンにはエチレングリコールが使用されていることもあるので要注意です。エチレングリコールはアルコール脱水素酵素・アルデヒド脱水素酵素により、有毒なグリコール酸やシュウ酸などに代謝されます。拮抗薬であるエタノールやホメピゾールはアルコール脱水素酵素に親和性が高く、有毒な代謝産物の産生を抑えることができます。最近はホメピゾールなどアルコール脱水素酵素阻害薬単剤でも透析なしで治療できることも多いというデータが出てきていますが、すでに代謝性アシドーシスが起きている場合(一つの目安としてAG24以上)にはホメピゾールだけでは治療が十分ではなく、透析をしてエチレングリコールやグリコール酸・シュウ酸などを除去する必要があります。(メタノールはエチレングリコールと違ってほとんどの場合に透析が必要になる点は似たような中毒でも大きな違いですね。)
認知症薬中毒(コリンエステラーゼ阻害薬中毒)
認知症の薬にはさまざまな種類がありますが、一番メジャーなものにコリンエステラーゼ阻害薬があり、ドネペジルやガランタミン、リバスチグミンがそれにあたります。
高齢の認知症を抱えた方が、自分で薬剤の管理を行っている場合には特に注意が必要です。
「内服薬を飲んだのに忘れてもう一度飲んでしまった。」「前日に貼った貼付剤を剥がし忘れて2枚目を貼ってしまった。」など意図的ではなく過量投与になってしまう可能性があります。
貼付剤は貼った後に1日経ってもまだかなりの薬剤が残っていることが知られており、これを繰り返すと効果が過剰になることがあります。
過剰なコリンエステラーゼ阻害薬の作用によって起こるのはコリン作動性のトキシドロームです。
徐脈・低血圧・発汗・意識障害・嘔吐・下痢・縮瞳などがそれにあたります。
とはいえ高齢者が徐脈・低血圧・発汗著明・意識障害で来院したら、多くの場合医療者は心原性ショックを考えると思います。
その時に、薬をレビューして身体所見で貼付剤が何枚も貼られていないかなど診るとともに、縮瞳・下痢など心原性ショックとはやや合致しない所見がないかどうかを確認することが大切になります。
殺鼠剤中毒(抗凝固薬)
殺鼠剤には抗凝固作用をメインにするものが多くあります。
ワーファリンと同じくVitamin K-1,25 epoxide reductaseを阻害し、Vitamin K依存性の凝固因子Ⅱ,Ⅶ,Ⅸ,Ⅹなどの産生が低下して抗凝固作用が出現します。
抗凝固系の殺鼠剤には第一世代と第二世代があり、第二世代は特にスーパーワーファリンと言われ、作用時間・半減期が極めて長いという特徴があります。血中濃度を測定することは通常できませんが、抗凝固作用はワーファリンと同様にPT-INRを測定することで可能です。
毒性としては脳出血などが起こるなど、易出血性が問題となります。通常は48時間以内にINRの延長作用がみられますが、スーパーワーファリンの中には効果出現までにより時間がかかることもあります。
一般には内服後48時間時点でINRが正常であれば中毒症状がでてくることは考えにくいです。治療はVitamin Kを補充することになりますが、ワーファリンであれば2.5−10mg/day程度で十分な効果を得られることが多いのに対して、スーパーワーファリンではその10倍以上の量が必要になることも多く、また治療期間も長期にわたります。
米国では最近合成大麻にスーパーワーファリンが混入していて、若い人たちの中毒が多発した事件が起こりました。誰が何の目的でスーパーワーファリンを入れたのかは未だに分かっていません。
アルコール中毒
アルコール中毒といえばもっとも皆さんがよく診察する機会のある中毒かもしれません。よく見る中毒でも実は… というようなピットフォールをお示しします。
①アルコール中毒は臭いを嗅げばわかる?
実は皆さんが感じるアルコール中毒の臭いはエタノールの臭いではないので、臭いで確実に診断できるという訳ではないので注意が必要です。
②血中アルコール濃度で症状は想定でき診断に重要
血中アルコール濃度を測定できる施設もあるかもしれませんが、血中アルコール濃度が同じであっても上昇している時の方が(飲み始め)、下がっている時の方が症状が軽くなります。(Mallenby効果)また人によって症状は大きく異なります。例えば血中アルコール濃度300mg/dlは普段飲酒されない方にとっては昏睡に至るような血中濃度ですが、普段から多くの飲酒をされている方にとっては普通に歩行できる程度の血中濃度であることもあります。ということで血中アルコール濃度の解釈には注意が必要です。
③点滴で症状回復を
よく知られているようにアルコールは主に肝臓で代謝されます、そのため補液を行ってもアルコール中毒の症状が早く改善するということはありません。脱水を合併していると考えられる場合には点滴が必要ですが、全例での点滴は必要ありません。
④合併症がないか、適切に診断を
アルコール中毒の患者様はビタミン欠乏や電解質異常、低血糖、頭部外傷などその他の合併症が隠れている可能性が高いです。全例で検査を行う必要はありませんが、適切な問診と診察で必要に応じて検査をする必要があります。
アセトアミノフェン中毒はなぜ起こる?
体内で代謝された為に毒物がたまる!!
アセトアミノフェンは解熱鎮痛薬として広く使われている薬剤です。治療量で使用された場合、アセトアミノフェンは主に肝臓でグルクロン酸抱合および硫酸抱合されて腎臓から排泄されます。一部の(約5-10%)アセトアミノフェンはCYP2E1で代謝されてNAPQIになります。このNAPQIこそが肝障害の一番の原因なのですが、このNAPQIはグルタチオンによって無毒化されます。アセトアミノフェンを大量に摂取すると、グルクロン酸抱合や硫酸抱合が間に合わなくなり、NAPQIが大量に発生します。また大量のNAPQIは量がおおいとグルタチオンによる無毒化が十分になされず、肝障害を起こします。(下記図参考)
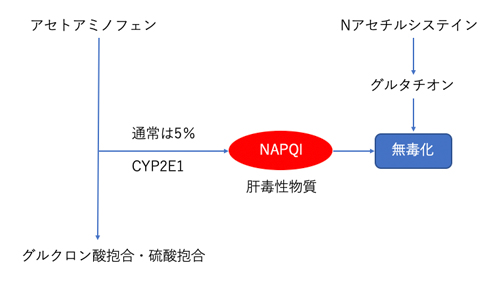
アセトアミノフェン中毒治療の切り札 Nアセチルシステイン
ありがたいことに、アセトアミノフェン中毒には非常に有効な拮抗薬Nアセチルシステインがあります。Nアセチルシステインは体内でグルタチオンを増加させてアセトアミノフェン中毒を防ぎます。Nアセチルシステインは摂取量が中毒量(体重当たり150-200mg/kg、または成人では10g以上)の場合や血中濃度がアセトアミノフェン中毒のノモグラムを上回る場合に投与します。140mg/kgを初回経口投与したのち、70mg/kgを4時間ごとに17回(総計18回)投与します。この拮抗薬は腐卵臭がしてかなり臭いのが問題です。ですが、早期に内服を開始すればほとんどの症例で肝障害を防ぐことができる非常に有効な治療となっています。ちなみに最近注目されているアセトアミノフェン中毒の拮抗薬にホメピゾール(本来はメタノールやエチレングリコールの拮抗薬)があります。ホメピゾールはCYP2E1をブロックするために有効になるとされています。
メトホルミン中毒:糖尿病治療薬中毒だけれども低血糖ではなく●●が問題に。
メトホルミンは2型糖尿病によく使用されるビグアナイドというクラスの薬剤です。
糖新生を抑え、末梢での糖の利用を促進し、脂肪酸β酸化を抑えるなど様々なメカニズムでその効果をもたらします。
中毒では低血糖を起こすことが少ないものの、ミトコンドリアの複合体Ⅰを阻害することなど様々なメカニズムで乳酸アシドーシスを起こすことがあります。
メトホルミンのほとんどは代謝されることなく、そのまま腎臓から排泄されます。
そのため、必ずしも大量に摂取していなくても腎臓の機能が悪化したせいで血中濃度が上昇して中毒になることがあります。
中毒では乳酸アシドーシスの他に、低血圧、呼吸不全、意識障害、多臓器不全を起こします。治療の基本は支持療法です。
重症のアシドーシス(pH < 7.1)、高乳酸血症(Lac > 20)、腎不全併発、支持療法で悪化する場合などには透析が適応になることもあります。
咳止めで一大事に?
咳止めに使用される薬にデキストロメトルファンがあります。
NMDA受容体のアンタゴニストとして作用します。メジコンという商品名で病院で処方されるほか、多くの市販薬に含まれていますが、実は麻薬に似た構造であり、乱用の恐れもあり注意が必要な薬です。
服用後はCYP2D6に代謝され活性型のデキストロルファンとなりますが、CYP2D6は遺伝子多型が多くあり、CYP2D6の活性が異常に高い方には少量の内服でも過剰に症状がでることがあります。
残念ながら誰がCYP2D6の高い活性を持っているかは事前には分からないのが難しいところです。
その他にデキストロメトルファンはセロトニンの再取り込みも抑制します。
もともとセロトニン症候群のリスクとなるような薬(SSRIなど)を飲んでいる方は飲み合わせにも要注意です。
ドパミンにも影響をおよぼすため中毒の際には特徴的な歩き方(足幅が広く、つま先を垂らす)をします。
中毒の症状として眼振、失調、意識障害、幻覚などがあります。
市販薬は安全と思いがちですが、思ってもみない副作用が出ることもあるので注意して下さい。
低血糖にサンドスタチン?
糖尿病の治療薬に使われるスルホニルウレア剤は膵臓の細胞で細胞内のカリウムの上昇をもたらします。
細胞内カリウムの上昇→細胞内のカルシウムの上昇→インスリン分泌となります。
サンドスタチンは細胞内にカルシウムが入ることを阻害し、結果としてインスリン分泌を抑えます。
この作用からスルホニルウレア剤による低血糖の際にサンドスタチンを50mcgを皮下注射にて対応することがあります。